サービス
ページ内目次
浜松ファーマリサーチの特長
創薬プロセス効率化のカギを握る「非臨床試験」
新たな医薬品の研究開発は、基礎研究で新薬候補物質(シーズ)を生み出すことを出発点に、その有効性・安全性を実験動物を用いて評価する「非臨床試験」、さらにヒトでの「臨床試験」で評価した後、新薬としての「承認申請」を行い、承認申請へと進みます。ひとつの医薬品が製品化される期間はおよそ9~17年。その間に500億円超の開発費を要すとされています。
しかし、臨床試験開始後の成功確率は減少傾向にあるといわれており、製薬企業の研究開発コストは増大、創薬の研究開発リスクの高まりが指摘されています。
しかし、臨床試験開始後の成功確率は減少傾向にあるといわれており、製薬企業の研究開発コストは増大、創薬の研究開発リスクの高まりが指摘されています。

「非臨床試験」は、実験動物を使用してシーズの有効性を評価し、その後安全性を確認する2段階に分かれています。
有効性を確認する「薬効薬理試験」では、一般的にマウス等の小動物が使用されることが多く、ヒトとの間には種差があり、非臨床試験で絞り込まれた新薬候補が臨床試験でヒトへの有効性を認められないことで開発中止となり問題化しています。
有効性を確認する「薬効薬理試験」では、一般的にマウス等の小動物が使用されることが多く、ヒトとの間には種差があり、非臨床試験で絞り込まれた新薬候補が臨床試験でヒトへの有効性を認められないことで開発中止となり問題化しています。
浜松ファーマリサーチはこの点に注目し、ヒトに近いサルを実験動物として使用することで種差を乗り越え、創薬プロセスの確実性を高めることができると考え、非臨床試験の「薬効薬理試験」に事業領域を特化して研究活動を精力的に行っています。
解剖学的にも生理学的にもヒトに最も近い実験動物「カニクイザル」

カニクイザルは、脳の構造と血管支配、そして二足歩行が可能など解剖学的にヒトに類似した霊長類です。また、タンパク質の構造等(抗体の認識性、血液成分)でも、ヒトに近似した研究に適しており、生理学的に安全性試験に古くから供用されてきましたが、薬効薬理試験での使用例は稀です。
サルによる薬効薬理試験が稀なのは、既存の病態モデルがほとんどないことや、ハンドリング可能な多数の研究者が必要、高額な研究費が必要なことが挙げられます。
サルによる薬効薬理試験が稀なのは、既存の病態モデルがほとんどないことや、ハンドリング可能な多数の研究者が必要、高額な研究費が必要なことが挙げられます。
当社では、霊長類のハンドリング技術に長けた優秀な薬理研究者が多数在籍しており、この分野に特化したビジネスモデルが高い競争力を保持しています。
受託可能な新病態モデル|日本から世界へ、NHPを用いた新規開発モデルを構築
当社で受託可能な非ヒト霊長類(NHP)を用いた病態モデルには、滲出型加齢黄斑変性、変形性膝関節症、抗がん剤誘発疼痛、FDA※が推奨する脳梗塞、ヒトと同じ4大症状が出現する唯一のモデルであるパーキンソン病、ヒトと血液成分の種差がない実験が行える血栓モデル等があります。開発中のパイプラインにおいては、潰瘍性大腸炎、萎縮型加齢黄斑変性、ドライアイ、痒みモデルなどがあります。今後さらに新領域へもチャレンジしてまいります。
※FDA(Food and Drug Administration of the United States Department of Health and Human Service):米国食品医薬品局。 日本の厚生労働省にあたる米国厚生省に属する。
※FDA(Food and Drug Administration of the United States Department of Health and Human Service):米国食品医薬品局。 日本の厚生労働省にあたる米国厚生省に属する。
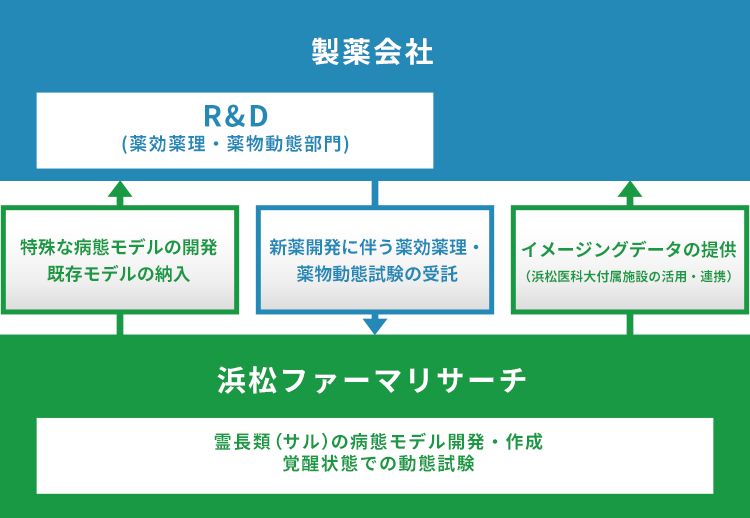
浜松ファーマリサーチは、主に非ヒト霊長類(NHP)を用いた非臨床試験に特化した創薬支援企業として、製薬会社のR&D部門から新規医薬品候補物質の薬効薬理・薬物動態試験を受託しています。
浜松医科大学との緊密な提携により、同大独自の「PIT法」を基幹技術に、既存/独自開発の病態モデルを用いた高精度な試験で得られたデータを納入。受託した候補物質の有効性が認められない場合にも、貴重なデータとしてその後の合理的かつスピーディな研究開発にご活用いただいています。
当社独自のNHPを用いた非臨床試験を中核とするビジネスモデルにより、創薬研究を支援し、さらには人類の健康に貢献してまいります。
浜松医科大学との緊密な提携により、同大独自の「PIT法」を基幹技術に、既存/独自開発の病態モデルを用いた高精度な試験で得られたデータを納入。受託した候補物質の有効性が認められない場合にも、貴重なデータとしてその後の合理的かつスピーディな研究開発にご活用いただいています。
当社独自のNHPを用いた非臨床試験を中核とするビジネスモデルにより、創薬研究を支援し、さらには人類の健康に貢献してまいります。
薬効薬理試験
脳梗塞や中枢神経性の疾患、難病など、現代において新薬が望まれる様々な領域において、私たちの薬効薬理試験が有効に実施されています。小動物はもとより、より人間に近い非ヒト霊長類(NHP)による実験・評価のフィードバックが、人類期待のさまざまな薬効薬理のイノベーションへと繋がります。小動物試験については、事業縮小を予定しております。小動物試験をご要望のお客様は、お問い合わせ下さい。
薬物動態試験もご依頼いただけます
サルを用いた薬物動態試験を実施しております。レンタルサルのご使用も可能です。
試験前日のプロトコール変更にも対応可能など、迅速な対応を心がけています。
カニクイザル薬物動態試験(PK試験)
試験前日のプロトコール変更にも対応可能など、迅速な対応を心がけています。
カニクイザル薬物動態試験(PK試験)
- 血漿サンプル採取
- 尿サンプル採取
- 髄液サンプル採取
- ブランク血漿の販売